Views: 12
| Imunizantes adquiridos pelo Brasil por meio de consórcio já estão sendo avaliados por técnicos da agência no âmbito internacional |
|---|
| SAÚDE | Do R7 09/02/2021 – 15H55 (ATUALIZADO EM 09/02/2021 – 17H34) |
| Quarta-feira, | atualiza 10 jfev de 2021 | 12h29 – Nazaré Paulista-SP – Por Editor: Bp Sérgio Oliveira |
| DIVULGAÇÃO |
____________________________________________________________________
“Portal de Notícias do Atitude News –, cria, edita ou altera o conteúdo exibido. Todo o processo de coleta de dados cujo resultado culmina nas informações a seguir é realizado automaticamente, através de fontes públicas pela Lei de Acesso à Informação (Lei Nº 12.527/2011). Portanto, Portal de Notícias do Atitude News –, não substitui as fontes originárias da informação, não garante a veracidade dos dados nem que eles estejam atualizados. O sistema pode mesclar homônimos (pessoas do mesmo nome). Confira nosso Descrição Legal.” [O jornalismo profissional precisa do seu suporte]. LEI Nº 12.527, DE 18 DE NOVEMBRO DE 2011. Regula o acesso a informações previsto no inciso XXXIII do art. … 216 da Constituição Federal; altera a Lei nº 8.112, de 11 de dezembro de 1990; revoga a Lei nº 11.111, de 5 de maio de 2005, e dispositivos da Lei nº 8.159, de 8 de janeiro de 1991; e dá outras providências. [O jornalismo profissional precisa do seu suporte].
_________________________________________________________________
Bem-vindo (a), ao Portal de Notícias do Atitude News.
A Diretoria Colegiada da Anvisa (Agência Nacional de Vigilância Sanitária) decidiu por unanimidade, nesta terça-feira (9), dispensar de registro ou autorização de uso emergencial vacinas contra covid-19 que o Brasil receberá por meio do consórcio Covax Facility.
Relatora da RDC (Resolução da Diretoria Colegiada), a diretora Meiruze Freitas afirmou que é “oportuno e atual o momento para aprimoramento de alguns procedimentos e diretrizes da regularidade sanitária, de forma a pavimentar o caminho para promovermos uma apropriada e célere disponibilização das vacinas objeto do acordo Covax Facility por todo o território nacional”.https://6d5009e1085be043274c79fb938e306e.safeframe.googlesyndication.com/safeframe/1-0-37/html/container.html
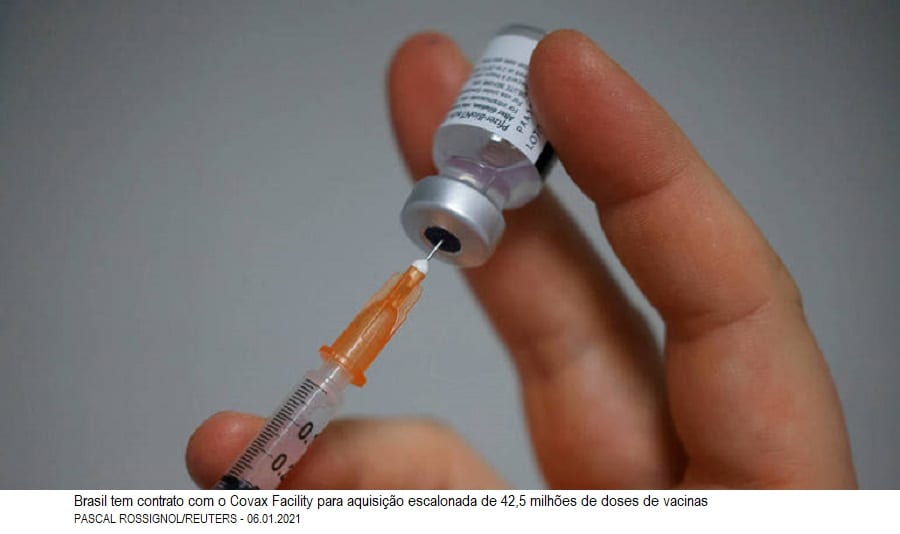
O Brasil tem acordo com o Covax Facility para aquisição escalonada de 42,5 milhões de doses de imunizantes que integram a iniciativa. As primeiras — da vacina Oxford/AstraZeneca — devem chegar a partir da metade do mês.
Com a decisão de hoje, não será necessária uma autorização de uso emergencial para os lotes serem importados, mas todos terão que passar por uma avaliação avaliação do INCQS (Instituto Nacional de Controle de Qualidade em Saúde), ligado à Fiocruz, antes de serem entregues ao PNI (Programa Nacional de Imunizações).
O diretor da Rômison Rodrigues Mota reforçou que a resolução facilita a chegada de mais vacinas ao Brasil.
“Se essa matéria não estivesse sendo trazida à apreciação desta Diretoria Colegiada, de forma, eu diria, antecipada, a cada lote dessas vacinas que chegasse ao Brasil, deveria ser precedida de uma deliberação desta agência. Da forma como estamos fazendo, já fica deliberada a entrada dessas vacinas no país.”
O Covax tem em seu portfólio diversas vacinas em estudo, algumas delas já aprovadas para uso emergencial, como a da Moderna e Oxford/AstraZeneca. A Pfizer aceitou recentemente fornecer vacinas ao programa.
Outros imunizantes promissores, como os desenvolvidos pela Novavax e CureVac também devem ser distribuídos por meio da iniciativa assim que os estudos estiverem concluídos.
Medida não afeta qualidade, segurança e eficácia
Os diretores da Anvisa ressaltaram que dispensar as vacinas do Covax de análise da agência brasileira não implica em flexibilizar exigências de qualidade segurança e eficácia dos produtos.
No entanto, como a OMS (Organização Mundial da Saúde) já tem um grupo de pré-qualificação e avaliação dos imunizantes do Covax Facility, é possível se basear nas análises da entidade.
Meiruze salientou que a decisão “é sustentada em uma avaliação que a Anvisa faz no âmbito do grupo de especialistas da Organização Mundial da Saúde”.
Ainda assim, foram impostas exigências ao Ministério da Saúde. As vacinas devem ser destinadas exclusivamente ao PNI.
A pasta deve também se responsável por todos os procedimentos para obter a licença de importação, assegurar condições da cadeia de transporte, além de mecanismos para garantir a qualidade dos imunizantes no armazenamento e prestar orientações aos serviços de saúde sobre os produtos.
A resolução permite que as vacinas sejam importadas com embalagens e rótulos em outros idiomas, desde que validados pela OMS.
NÃO HÁ JUSTIÇA SEM DEUS
- Precisando de ajuda? ☎ Ligue para: (11) 4260-0540 |
- WhatsApp: (11) 97228-2486 | 97066-8705 |
- Fale com Bp Sérgio J. Oliveira – Editor Jornalista agora mesmo: !
- E-mails.: [email protected] | [email protected] |
- [email protected] | [email protected]









